牛磺熊去氧胆酸TUDCA对新冠肺炎(COVID-19)的治疗潜力
牛磺熊去氧胆酸TUDCA对新冠肺炎(COVID-19)的治疗潜力
前言:
新型冠状病毒肺炎(Corona VirusDisease 2019,COVID-19),简称“新冠肺炎”,是指2019年新型冠状病毒感染导致的肺炎。
COVID-19不仅攻击肺,还累及心脏、肾脏、肝脏。患者如果最终发展成为呼吸衰竭,心脏、肾脏、肝脏等器官都会出问题,导致多器官功能衰竭。牛磺熊去氧胆酸(tauroursodeoxycholic,TUDCA)具有多重药理作用,广泛应用于肝、胆疾病的治疗[1,2],并应用于神经退行性疾病,并开展了肌萎缩侧索硬化(amyotrophiclateral sclerosis,ALS)的三期临床研究[3]。在临床与临床前研究中,可以看到TUDCA具有保护多种脏器的作用,基于这些研究,可以推断TUDCA在COVID-19的治疗中有较大的应用价值。
1.TUDCA抑制内质网应激诱导的细胞凋亡
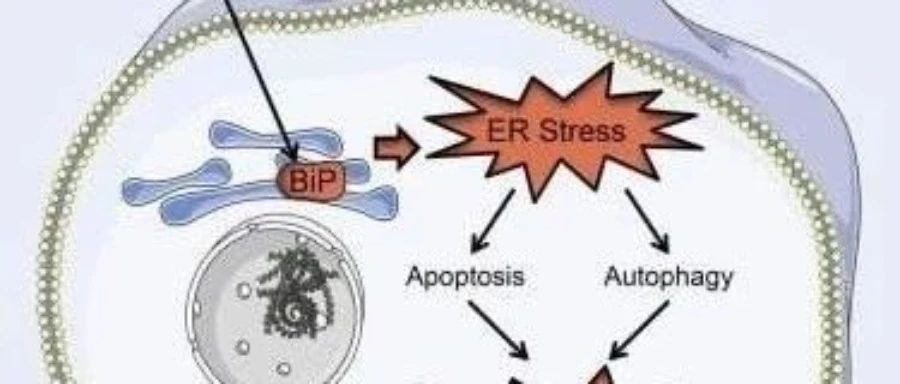
在真核细胞中,内质网作为蛋白质折叠和翻译后修饰的重要场所,是许多病毒复制和成熟的必需细胞器。感染冠状病毒后,病毒蛋白在内质网上的大量合成折叠和修饰、病毒基因组复制时形成的双层膜囊泡(DMVs)导致的大量膜的重排、病毒粒子出芽和诱导自噬导致的内质网膜的消耗均会增加内质网的负担,进而增加了未折叠蛋白和错误折叠蛋白的堆积,因此,感染冠状病毒后通常会诱发内质网应激(ERS),激活非折叠蛋白应答(UPR)。UPR虽然可以改变细胞的转录和翻译程序,来以缓解ERS保护细胞,但是,严重的内质网应激可以激活促炎细胞因子,造成炎症反应,甚至可以启动细胞凋亡,造成细胞的死亡[4,5]。内质网应激是细胞凋亡的第三条通道,另外两条分别是研究较为广泛的死亡受体通道和线粒体通道。TUDCA对三条通道诱导的细胞凋亡均有抑制作用。
化学分子伴侣是一组小分子量的化合物,能稳定蛋白的折叠和缓冲异常蛋白的堆积。化学分子伴侣通过减少蛋白错误折叠、提高内质网折叠功能,从而减轻ERS。体外研究较充分的化学分子伴侣是4-苯丁酸(4-PBA)和牛磺熊去氧胆酸(TUDCA) [6]。它们已经分别用于治疗尿素循环障碍和胆石症、胆汁淤积性肝病。虽然二者都可以抑制内质网应激,但与4-PBA不同的是,TUDCA可以保护细胞的生存能力,4-PBA却会降低细胞的生存能力[7]。
2.TUDCA应用于感染性疾病的治疗
TUDCA最早应用于病毒性肝病的治疗,单药治疗HBV、HCV的患者,肝脏生化指标和免疫学指标均得到改善[8]。针对肝硬化患者的治疗,表现出了组织学改善的趋势[9]。在动物实验中,可以看到TUDCA具有明确的抑制四氯化碳诱导的肝纤维化的作用[10]。体外研究显示,TUDCA可以破坏甲型流感病毒M2质子通道,以此来抑制病毒感染,同时TUDCA可以减轻感染带来的肺上皮细胞损伤[11]。
另外一项研究显示,TUDCA可以通过阻断内质网应激的IRE1通路,抑制甲型流感病毒的复制[12]。同样,TUDCA也可以抑制柯萨奇病毒感染引起的内质网应激及心肌炎症[13]。
3.TUDCA应用于非感染性疾病的治疗,可以保护多种器官。
新冠病毒患者肝功能异常率为43.4% (43/99) [14],主要原因是新冠病毒特异性攻击胆管细胞(ACE2高表达),造成胆管细胞损伤。TUDCA促进胆汁分泌,促进胆管细胞分泌重碳酸盐,保护胆管细胞,临床上已经常规用于PBC(胆管损伤疾病)的治疗 。
TUDCA对细胞凋亡的三条通( 细胞外死亡受体通路,细胞内线粒体和内质网应激通路)均有抑制作用,在体外实验中,也证实TUDCA对细胞凋亡引起的的心脏[15],肺[16,17],肾脏[18],胰腺[19]损伤均有抑制作用。并证实TUDCA具有抗炎效果[20,21,22],是一个有效的细胞保护剂。其中,体外研究显示防治肺纤维化效果显著优于临床上已经用于新冠肺炎治疗的氯喹[23],展现了对多种疾病治疗的潜力。
TUDCA在退行性疾病的研究中显示对阿尔茨海默症[24],亨廷顿舞蹈症[25],视网膜变性[26], 肌萎缩侧索硬化(amyotrophic lateral sclerosis,ALS)具有治疗潜力。
肌萎缩侧索硬化(amyotrophic lateral sclerosis,ALS)最显著的病理改变是选择性的运动神经元损害。最近研究表明,运动神经元的缺失主要是由凋亡引起的。变异的过氧化物歧化酶1(superoxide dismutase 1,SOD1)通过不确切的机制进入内质网形成蛋白聚集物,和其他不明确的原因引起内质网应激和未折叠蛋白反应,进而通过激活Caspase-12、凋亡信号调节激酶(apoptosis-signal regulatingkinase 1,ASK1)-c-Jun氨基末端激酶(c-Jun-NH2-terminalkinases,JNK)通路、CHOP表达升高、钙离子的释放,引起运动神经元的凋亡[27]。
TUDCA在治疗ALS的二期临床研究中,显示其在较高剂量(2g/天)治疗与内质网应激相关的神经系统疾病中是有效和安全的[28],目前针对该疾病治疗的三期临床研究正在开展。
4. TUDCA用于房尘螨诱导的过敏性气道疾病的研究
研究者通过房尘螨(HDM)诱导的小鼠过敏性气道疾病模型[29],使用牛磺熊去氧胆酸(TUDCA),测试其治疗过敏性哮喘的效果。
研究发现TUDCA减少了HDM引起的气道炎症、粘液化生、内质网应激标记物和气道高反应性(AHR)和纤维化水平,对气道重塑则无影响。比较重要的是,该实验模型中,TUDCA下调了粘液因子Muc5ac, Gob5, 和 Xbp1s的mRNA水平,可能对炎症状态下肺部粘液生成有一定抑制作用。
目前,欧洲计划开展TUDCA治疗哮喘的临床研究[30],用药剂量为1750mg/d,早500mg( 2粒250mg胶囊),中午500mg(2粒250mg胶囊),晚上750mg( 3粒250mg胶囊),这对其临床应用可能会有一定借鉴意义。
总结:
TUDCA虽然不能在核酸水平上对病毒的复制进行抑制,却可以在蛋白水平上抑制病毒的感染能力,抑制病毒的复制及感染诱导的损伤。TUDCA除了作为胆固醇的溶剂,也是一个信号分子,在多个信号通路中,发挥调控作用,发挥多重药理作用,是一个广泛范围的细胞保护剂,并具有良好的安全性。
TUDCA作为一种化学分子伴侣,具有抗内质网应激的作用,可以调控病毒的复制,并可降低炎性因子水平,在应对感染带来的细胞因子风暴炎症反应中,具有保护多种脏器的作用,据此推断TUDCA在应对COVID-19的治疗中,具有较大的应用价值。
参考文献:
1.傅贤波,林三仁,范竹萍,邱德凯,牛磺熊去氧胆酸溶解胆固醇结石有效性和安全性随机、双盲、安慰剂对照多中心临床研究,中国微创外科杂志,2007年12月第7卷第12期
2. Hong Ma,Jidong Jia,et.al.Amulticenter,randomized,double-blind trial comparing the efficacy and safety ofTUDCA and UDCA in Chinese patients with primary biliary cholangitis.Medicine(2016)95:47
3. clinicaltrials NCT03800524
4.Xue Mei,Fu.Fang,Ma Yan.1ong,et a1.The PERK Arm of the Unfolded ProteinResponse Negatively Regulates Transmissible Gastroenteritis Virus Replicationby Suppressing Protein Translation and Promoting Type I IFN Production,J Virol,2018
5.ToS.Fung andDingX.Liu Coronavirus infection, ERstress,apoptosis and innateimmunity,Frontiersin Microbiology Virology
6.郭媛媛,任锋综述,段钟平,张桓虎审校,内质网应激诱导未折叠蛋白反应干预药物作用研究进展,实用肝脏病杂志
7.JagadeeshKumar Uppala,et al,Chemical chaperone, TUDCA unlike PBA, mitigates proteinaggregation efficiently and resists ER and non-ER stress induced HepG2 cell,www.nature.com/scientificreports
8. Leonardo Furio,Treatment of virus-assocaitedliver cirrhosis with tauroursodeoxycholic acid: evalution of cytolysis andcholestasis indexes and selected immunologic variables, Current TherapeuticResearch,1994
9.王丹, 杨玲等,牛磺熊去氧胆酸抑制四氯化碳诱导的大鼠肝纤维化,世界华人消化杂志
10.Xiao-liPAN,Xiao-hua HOU,et al,Efficacy and Safety of Tauroursodeoxycholic Acid in theTreatment of Liver Cirrhosis: A Double-blind Randomized Controlled Trial ,JHuazhong Univ Sci Technol[Med Sci]
11.Ning Li,Chengyu Jiang,Tauroursodeoxycholic acid (TUDCA) inhibits influenza A viralinfection by disrupting viral proton channel M2
12.Ihab H. Hassan et al.Influenza A ViralReplication Is Blocked by Inhibition of the
13.Xi Zha , Yan Yue,et al.Endoplasmic ReticulumStress Aggravates Viral
Myocarditis by Raising Inflammation Through the IRE1-Associated NF-κB Pathway,Canadian Journal of Cardiology
14.Epidemiological and clinical characteristicsof 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: a descriptivestudy
15ShilpaRani,et al.Tauroursodeoxycholic acid (TUDCA) attenuates pressureoverload-induced cardiac remodeling by reducing endoplasmic reticulumstress,PLOS ONE
16. Yuta Tanaka, Yoichi Ishitsuka,etal.The exacerbating roles of CCAAT/enhancer-binding proteinhomologous protein(CHOP) in the development ofbleomycin-induced pulmonary fibrosis and thepreventiveeffects of tauroursodeoxycholic acid (TUDCA) againstpulmonaryfibrosis in mice.
17.Broccard et al. Tauroursodeoxycholic acidinhibits apoptosis associated with ventilator-induced lung injury in rabbits.OA Critical Care 2013 Jul 01;1(2):11.
18.Jing Zhang,Ying Fan,et al. Tauroursodeoxycholic Acid Attenuates Renal Tubular Injury in aMouse Model of Type 2 Diabetes,Nutrients.
19.Ersin Seyhun,Antje Malo,et al,Tauroursodeoxycholic acid reduces endoplasmic reticulumstress, acinar cell damage, and systemic inflammation in acutepancreatitis,AJP-Gastrointest Liver Physiol
20.Seong Jun Kim et al,Anti-inflammatory effectof Tauroursodeoxycholic acid in RAW 264.7 macrophages, Bone marrow-derivedmacrophages, BV2 microglial cells, and spinal cordinjury.www.nature.com/scientificreports
21.Natalia Yanguas-Casás,Tauroursodeoxycholicacid reduces glial cell activation in an animal model of acuteneuroinflammation.JOURNAL OF NEUROINFLAMMATION
22. Kim YH, et al,Tauroursodeoxycholic acidattenuates colitis-associated colon cancer by inhibiting nuclear factor kappaBsignaling. J Gastroenterol Hepatol. 2019
23.朱锦东,蒋澄宇等,牛磺熊去氧胆酸减轻TGF-β1诱导的MRC-5纤维化表型,基础医学与临床 2015
24. R. J. S. Viana, A. F.Nunes,Tauroursodeoxycholic acid prevents E22Q Alzheimer’s Aβ toxicity in humancerebral endothelial cells,Cell Mol Life Sci. 2009
25.C. Dirk Keene, Cecilia M. P. Rodrigues etal,Tauroursodeoxycholic acid, a bile acid, is neuroprotective in a transgenicanimal model of Huntington’s disease,PNAS
26.Noailles A,et al,Microglia activation in a model of retinal degeneration and TUDCAneuroprotective effects.J Neuroinflammation.
27.张蔷等,内质网应激和肌萎缩侧索硬化,医学研究生学报
28.A. E. Eliaa,*, S. Lalli,Tauroursodeoxycholicacid in the treatment of patients with amyotrophic lateral sclerosis,European Journal of Neurology 2015
29.Jalahalli M.etal,Effect of a chemical chaperone, auroursodeoxycholic acid, on HDM-induced allergicairway disease
30.https://www.clinicaltrials.gov/ct2/show/NCT03878654
上一篇: 名医讲堂—胡海:保胆的艺术
下一篇: 肠道菌群通过影响胆汁酸代谢参与胆囊胆固醇
