药物性肝损伤诊治指南(2015年版)
一、背景
药物性肝损伤(drug-induced liver injury,DILI)是指由各类处方或非处方的化学药物、生物制剂、传统中药(TCM)、天然药(NM)、保健品(HP)、膳食补充剂(DS)及其代谢产物乃至辅料等所诱发的肝损伤[1-4]。TCM 是指在我国中医等传统民族医药学理论指导下生产和使用的各种草药和非草药类的中药材、饮片和复方中成药,NM 是指应用现代医药理论和技术制备的天然药用物质及其制剂。DILI 是最常见和最严重的药物不良反应(ADR)之一[1,5],重者可致急性肝衰竭(ALF)甚至死亡[6]。 迄今仍缺乏简便、客观、特异的诊断指标和特效治疗手段。
美国于 2003 年创立了 DILI 协作网络(DILIN),2004 年启动了 DILIN 前瞻性研究(DILIN-PS)[2]。 2012 年发布了 LiverTox 网站(http://www.livertox.nih.gov)[7],2014 年美国胃肠病学会(ACG)基于有限证据出台了全球首个针对特异质型 DILI(IDILI)的临床指南[3]。我国于 2014 年发布了中国 HepaTox 网站(http://www.hepatox.org)[8]。LiverTox 和 HepaTox 网站分别记录了近 700 种和 400 余种常见药物的肝损伤信息,为临床医生慎重处方具有潜在肝毒性的药物及评估其风险和收益提供了重要依据。
近年来国内有多个非肝病专业学会发布了各自领域的 DILI 相关专家共识,但相应的证据选择和评估标准欠规范。为提高我国临床医生对 DILI 的认知并开展相关科研工作,避免诊疗实践中的困惑,中华医学会肝病学分会组织国内有关专家系统总结了国内外研究进展,力求公正和客观地起草了本指南。本指南适用于固有型 DILI(intrinsic DILI,InDILI)和 IDILI 的防治。根据循证医学原则,对涉及 DILI 临床诊治的部分提出了相关建议。随着 DILI 研究新证据的确认,指南将适时更新。
本指南采用 GRADE 系统对推荐意见的级别(见表 1)和循证医学证据的质量(见表 2)进行评估。在形成推荐意见时,不仅考虑到证据的质量,还要权衡干预的利弊与负担、患者偏好和价值观的可
变性,以及资源的合理利用、推荐措施的公平性与可实施性等。


二、流行病学
(一)发病率和流行趋势
在发达国家,DILI 发病率估计介于 1/100 000~20/100 000 或更低[1,9]。2002 年法国报道 DILI 年发病率约为 13.9/100 000,2013 年冰岛报道 DILI 年发病率约为 19.1/100 000[1,10]。我国目前报道的 DILI 发病率主要来自相关医疗机构的住院或门诊患者[6,11,12],其中急性 DILI 约占急性肝损伤住院比例的 20%[6];由于缺乏面向普通人群的大规模 DILI 流行病学数据,故尚不清楚 DILI 在人群中的确切发病率。
我国人口基数庞大,临床药物种类繁多,人群不规范用药较为普遍,应用 TCM-NM-HP-DS 等较为随意,医务人员和公众对药物安全性问题和 DILI 的认知尚不够,因此 DILI 发病率有逐年升高趋势[6]。又由于各地药物种类、用药习惯(剂量和疗程)、ADR 报告制度执行力的差异,以及不同地区、不同种族及不同人群药物代谢酶的基因多态性等[9],使得 DILI 的种类和发病率也可能存在地区差异[6,11,12]。
(二)引起 DILI 的药物
已知全球有 1100 多种上市药物具有潜在肝毒性,常见的包括非甾体类抗炎药(NSAIDs)、抗感染药物(含抗结核药物)、抗肿瘤药物、中枢神经系统用药、心血管系统用药、代谢性疾病用药、激素类药物、某些生物制剂和 TCM-NM-HP-DS 等[3,10]。不同药物可导致相同类型肝损伤,同一种药物也可导致不同类型的肝损伤,详细信息参见 LiverTox 和 HepaTox 网站。
在欧美发达国家,NSAIDs、抗感染药物、草药和膳食补充剂(HDS)是导致 DILI 的常见原因。其中,对乙酰氨基酚(APAP)是引起 ALF 最主要的原因[13,14]。TCM-NM-HP-DS 或 HDS 作为 DILI 的病因在全球越来越受到重视。2013 年冰岛一项前瞻性研究表明该国 HDS 占 DILI 病因的 16%[1],美国 DILIN 数据显示 HDS 占 DILI 病因的 20%以上。国内有报道相关药物涉及 TCM(23%)、抗感染药(17.6%)、抗肿瘤药(15%)、激素类药(14%)、心血管药物(10%)、NSAIDs(8.7%)、免疫抑制剂(4.7%)、镇静和神经精神药物(2.6%)等[6]。
国内报道较多的与肝损伤相关的 TCM-NM-HP-DS 有何首乌、土三七,以及治疗骨质疏松、关节炎、白癜风、银屑病、湿疹、痤疮等疾病的某些复方制剂等。但由于组分复杂,很难确定究竟是哪些成分引 起肝损伤[3]。我国中成药被要求按照《药品注册管理办法》完成药学、药理、毒理和临床研究,经严格 评审合格后方可批准上市。《药典》规定,除药食两用的饮片外,中药饮片均按照处方药进行管理。虽然 中成药、中药饮片均须按照《药品生产管理规范》(GMP)和《药品经营质量管理规范》(GSP)进行生产和销售,但中药汤剂和膏方作为处方药,医生可以开出不同组合的 TCM-NM 而无需批准。此外,很多属于非处方药的 TCM-NM 和民间 TCM 验方应用十分普遍,且 HP-DS 更是易于购得。在美国,绝大多数 HDS 未按照药品标准研发,无需临床前和临床安全性及有效性验证,也无需通过食品和药物管理局(FDA)批准即可上市[7]。以上因素均增加了滥用 TCM-NM-HP-DS 或 HDS 引起 DILI 的风险。因此, 欧盟已要求 HDS 应严格按照《欧盟传统草药产品指令》注册后方可上市。
(三)危险因素
1.宿主因素 包括遗传学因素和非遗传学因素。
遗传学因素主要是指药物代谢酶、药物转运蛋白和人类白细胞抗原系统(HLA)等的基因多态性与DILI 相关[3]。不同种族的患者对 DILI 的易感性可能存在差异[15]。
非遗传学风险因素众多(如下),但尚未发现其中任何一种是所有 DILI 的主要风险因素。
(1)年龄:高龄可能是 DILI 的重要易感因素[16]。但冰岛前瞻性研究提示,高龄患者的处方量增加可能是其 DILI 发生率相对较高的一个因素[17]。
(2)性别:女性可能对某些药物,如米诺环素、甲基多巴等表现出更高的易感性,且易于呈现慢性自身免疫性肝炎(AIH)的特点[18]。TCM-NM-HP-DS[19]引起的肝损伤在女性中也更多见。
(3)妊娠:妊娠期 DILI 常见可疑药物有甲基多巴、肼苯达嗪、抗生素、丙基硫氧嘧啶(PTU)及抗逆转录病毒药物(ART)等。PTU 可致孕妇暴发性肝炎,病死率高[20],FDA 已给予黑框警示。
(4)基础疾病:有慢性肝病基础的患者更易发生 DILI 的证据有限。但一旦发生,出现肝功能衰竭甚至死亡的风险更高[21]。有研究提示,乙型肝炎病毒(HBV)或丙型肝炎病毒(HCV)感染可增加 ART 或抗结核药发生 DILI 的风险。人类免疫缺陷病毒(HIV)感染是某些 DILI 的易感因素,也是影响 HIV 感染者 DILI 发病率和病死率的重要因素[22,23]。
自身免疫性肝病也可能增加患者对 DILI 的易感性,特别是使慢性 DILI 的发生风险增加[24]。尚不清楚非酒精性脂肪性肝病(NAFLD)和肥胖是否增加 DILI 的风险[25]。糖尿病是某些药物引起 DILI 的易感因素,有研究提示糖尿病与 DILI 严重程度独立相关。肿瘤及心脏病也是慢性 DILI 的可能危险因素[15]。
2. 药物因素 药物的化学性质、剂量、疗程,以及药物相互作用常可影响 DILI 的潜伏期、临床表型、病程和结局。一种药物可改变其他药物的吸收、分布、代谢、排泄和药理作用。药物相互作用是临床上 DILI 风险增加不容忽视的因素,如当抗结核药物与唑类抗真菌药、甲氨蝶呤、抗痉挛药、氟烷或APAP 等药物同时使用时,DILI 的发生率将增加[26,27]。中药材种植和炮制等过程中的污染也是增加 DILI发生风险的重要因素。
3. 环境因素 过量饮酒可能增加度洛西汀、APAP、甲氨蝶呤及异烟肼等引起 DILI 的风险[3]。吸烟对 DILI 易感性的影响尚不清楚。
DILI 发病机制复杂,往往是多种机制先后或共同作用的结果,迄今尚未充分阐明。通常可概括为药物的直接肝毒性和特异质性肝毒性作用,其过程包括药物及其代谢产物导致的“上游”事件以及肝脏靶细胞损伤通路和保护通路失衡构成的“下游”事件。
药物的直接肝毒性是指摄入体内的药物和/或其代谢产物对肝脏产生的直接损伤,往往呈剂量依赖性,通常可预测,也称固有型 DILI[32,33]。药物的直接肝毒性可进一步引起免疫和炎症应答等其他肝损伤机制。
特异质性肝毒性的发生机制是近年的研究热点。药物代谢酶系(细胞色素 P450 等Ⅰ相代谢酶系和多种Ⅱ相代谢酶系)、跨膜转运蛋白(ATP 结合盒 B11 等)及溶质转运蛋白(阴离子转运多肽 1B1 等) 的基因多态性可导致这些酶或转运蛋白功能异常[34-37],而 HLA 的基因多态性可导致对某些药物较易产生适应性免疫应答[38],这些基因多态性及其表观遗传特点可增加宿主对 DILI 的易感性。药物及其活性代谢产物诱导的肝细胞线粒体受损和氧化应激可通过多种分子机制引起肝细胞损伤和死亡[39-47]。持久和 过强的内质网应激反应(ERSR)将打破非折叠蛋白反应(UPR)对应激的缓解效应,促进 DILI 进展[48-52]。药物及其代谢产物可活化多种死亡信号通路,促进细胞凋亡、坏死和自噬性死亡的发生[53-56]。适应性免 疫攻击可能是 DILI 的最后共同事件。首先,细胞损伤和死亡所产生的危险信号可活化抗原递呈细胞而诱导适应性免疫攻击。其次,许多药物代谢产物可能作为半抗原与宿主蛋白结合形成新抗原。若适应性免 疫应答针对新抗原中的宿主蛋白,将导致自身免疫应答;若识别新抗原中药物代谢产物,将导致抗药物免疫应答[57-63]。此外,适应性免疫应答不仅可以介导 IDILI,还可能引起肝外免疫损伤,产生发热和皮疹等全身性表现。炎症应答主要是与免疫激活及一系列相关细胞和分子事件的组合,炎症和药物暴露的 相互作用是 DILI 发病机制的重要假说之一。外源性炎症既是 DILI 的独立易感因素,也是促使 DILI 进展的因素[64];而药物或其代谢产物也可激发肝内炎症应答,促使 DILI 进展[64-68]。最后需要指出,药物在启动肝损伤的同时也将激发恢复性组织修复(RTR)[69,70]。肝损伤启动后,若 RTR 缺乏则损伤迅速进展, 若 RTR 及时而充分则能限制和逆转肝损伤。因此,RTR 是肝损伤进展或消退的内在决定性因素[70]。
(一)DILI 的临床分型
1. 固有型和特异质型
是基于发病机制的分型。固有型 DILI 具有可预测性,与药物剂量密切相关,潜伏期短,个体差异不显著。固有型 DILI 已相对少见,除非收益明显大于风险的药物,才能批准上市。特异质型(IDILI)具有不可预测性,现临床上较为常见,个体差异显著,与药物剂量常无相关性,动物 实验难以复制,临床表现多样化[32]。多种药物可引起 IDILI[3,77]。
IDILI 又可分为免疫特异质性 DILI 和遗传特异质性 DILI。免疫特异质性 DILI 有两种表现,一是超敏性,通常起病较快(用药后 1~6 周),临床表现为发热、皮疹、嗜酸性粒细胞增多等,再次用药可快速导致肝损伤;另一种是药物诱发的自身免疫性损伤,发生缓慢,体内可能出现多种自身抗体,可表现为 AIH 或类似原发性胆汁性胆管炎(PBC)和原发性硬化性胆管炎(PSC)等自身免疫性肝病,多无发热、皮疹、嗜酸性粒细胞增多等表现。遗传特异质性 DILI 通常无免疫反应特征,起病缓慢(最晚可达 1 年左右),再次用药未必快速导致肝损伤[3,77]。
2. 急性 DILI 和慢性 DILI
是基于病程的分型。本指南采用的慢性 DILI 定义为:DILI 发生 6 个月后,血清 ALT、AST、ALP 及 TBil 仍持续异常,或存在门静脉高压或慢性肝损伤的影像学和组织学证据[2,3,78]。在临床上,急性 DILI 占绝大多数,其中 6%~20%可发展为慢性 [15,79-81]。有研究显示,急性 DILI发病 3 个月后约 42%的患者仍存在肝脏生化指标异常,随访 1 年约 17%的患者仍存在肝生化指标异常[82]。胆汁淤积型 DILI 相对易于进展为慢性[24]。
3. 肝细胞损伤型、胆汁淤积型、混合型和肝血管损伤型
是基于受损靶细胞类型的分类。由国际医学组织理事会(CIOMS)初步建立、后经修订的前三种 DILI 的判断标准为[3,77,83]:
(1)肝细胞损伤型:ALT ≥3 ULN,且 R≥5;
(2)胆汁淤积型:ALP ≥2 ULN,且 R≤2;
(3)混合型:ALT≥3 ULN,ALP≥2 ULN,且 2<R<5。若 ALT 和 ALP 达不到上述标准,则称为“肝脏生化学检查异常”。
R=(ALT 实测值/ALT ULN)/(ALP 实测值/ALP ULN)。
在病程中的不同时机计算 R 值,有助于更准确地判断 DILI 的临床类型及其演变。新近有研究提出“新 R 值(new R, NR)”,与 R 的不同是取 ALT或 AST 两者中的高值进行计算[84]。胆汁淤积型 DILI 约占 DILI 总数的 30%,有认为此估算可能偏低[69]。
肝血管损伤型 DILI 相对少见,发病机制尚不清楚,靶细胞可为肝窦、肝小静脉和肝静脉主干及门静 脉等的内皮细胞,临床类型包括肝窦阻塞综合征/肝小静脉闭塞病(SOS/VOD)[85,86]、紫癜性肝病(PH)[87,88]、巴德-基亚里综合征(BCS)、可引起特发性门静脉高压症(IPH)的肝汇管区硬化和门静脉栓塞、肝脏结节性再生性增生(NRH)等[71]。致病药物包括含吡咯双烷生物碱的草药、某些化疗药、同化激素、避孕药、免疫抑制剂及 ART 等,其靶向的血管内皮细胞各有不同或存在交叉。例如,SOS/VOD 与肝窦和肝脏终末小静脉内皮的损伤有关,临床上主要由大剂量放化疗[86]以及含吡咯双烷生物碱的植物如土三 七等引起[85]。土三七等引起的 SOS/VOD 近 10 年来我国已报道 100 余例。应注意感染、免疫紊乱、各种能导致血液高凝、高粘或促血栓形成的因素、微量元素异常及肿瘤等也可引起肝血管损伤,这些因素可 单独或共同起作用。
4. DILI 相关肝脏良性和恶性肿瘤
(二)DILI 的临床表现
急性 DILI 的临床表现通常无特异性。潜伏期差异很大,可短至 1 至数日、长达数月。多数患者可无明显症状,仅有血清 ALT、AST 及 ALP、GGT 等肝脏生化指标不同程度的升高。部分患者可有乏力、食欲减退、厌油、肝区胀痛及上腹不适等消化道症状[3,6]。淤胆明显者可有全身皮肤黄染、大便颜色变浅和瘙痒等。少数患者可有发热、皮疹、嗜酸性粒细胞增多甚至关节酸痛等过敏表现,还可能伴有其他肝外器官损伤的表现。病情严重者可出现 ALF 或亚急性肝衰竭(SALF)。
慢性 DILI 在临床上可表现为慢性肝炎、肝纤维化、代偿性和失代偿性肝硬化、AIH 样 DILI、慢性肝内胆汁淤积和胆管消失综合征(VBDS)等。少数患者还可出现 SOS/VOD 及肝脏肿瘤等[77]。SOS/VOD 可呈急性,并有腹水、黄疸、肝脏肿大等表现[77]。
当前,DILI 的诊断仍属排他性诊断。首先要确认存在肝损伤,其次排除其他肝病,再通过因果关系评估来确定肝损伤与可疑药物的相关程度。
(一)诊断要点
1. DILI 发病时间差异很大,与用药的关联常较隐蔽,缺乏特异性诊断标志物。因此全面细致地追溯可疑药物应用史和除外其他肝损伤病因,对于建立 DILI 诊断至关重要。
2. 当有基础肝病或多种肝损伤病因存在时,叠加的 DILI 易被误认为原有肝病的发作或加重,或其他原因引起的肝损伤。DILI 患者中既往有肝病史者超过 6%[80];而既往有肝病史的患者约 1%可出现DILI[101]。如 HBV 或 HCV 感染者合并炎症性肠病(IBD)应用免疫抑制剂治疗易发生肝损伤[102],往往很难鉴定是由免疫抑制治疗导致病毒激活,还是 IBD 合并的自身免疫性肝损伤,或由于免疫抑制药物导致的 DILI,甚或这三种情况同时发生。因此,当存在多种可能病因时,仔细甄别肝损伤的最可能原因非常重要。有研究认为发生在已有肝病基础上的 DILI 发病率和严重程度均可能被低估。
3. 鉴于部分患者表现为药物性自限性轻度肝损伤(适应)[103],此后可自行完全恢复。为避免不必要的停药,国际严重不良反应协会(iSAEC)于 2011 年将 DILI 的生化学诊断标准建议调整为出现以下任一情况[104]:(1)ALT≥ 5 ULN;(2)ALP≥ 2 ULN,特别是伴有 5′-核苷酸酶或 GGT 升高且排除骨病引起的 ALP 升高;(3)ALT≥ 3 ULN 且 TBil≥ 2 ULN。需要指出,此非 DILI 的临床诊断标准,而主要是对治疗决策更具参考意义。
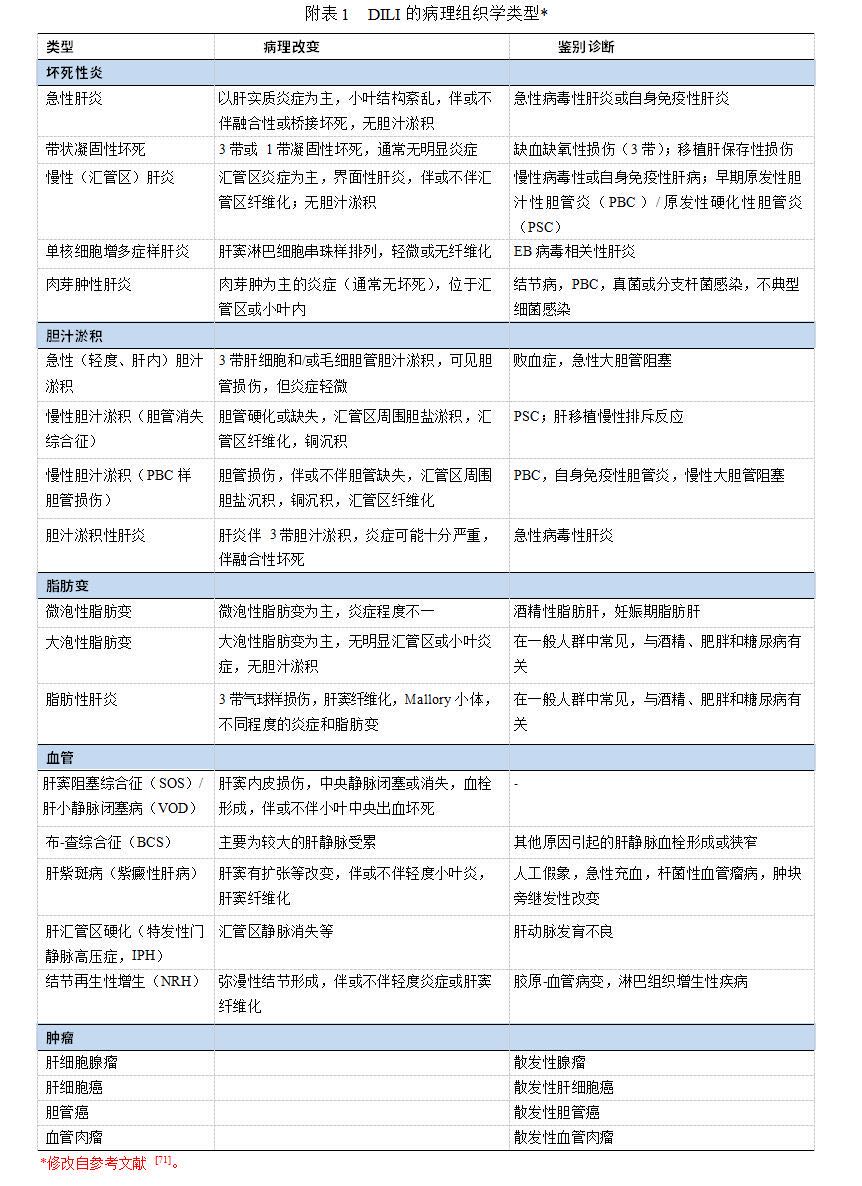
4. 下列情况应考虑肝组织活检:(1)经临床和实验室检查仍不能确诊 DILI,尤其是 AIH 仍不能排除时;(2)停用可疑药物后,肝脏生化指标仍持续上升或出现肝功能恶化的其他迹象;(3)停用可疑药物 1~3 个月,肝脏生化指标未降至峰值的 50%或更低;(4)怀疑慢性 DILI 或伴有其他慢性肝病时;(5)长期使用某些可能导致肝纤维化的药物,如甲氨蝶呤等。
(二)因果关系评估方案
DILI 的诊断评估方案主要有 Roussel Uclaf 因果关系评估法(RUCAM)[105]。RUCAM 由 CIOMS 在1989 年首次推出,1993 年修改完善(称为 Danan 方案)[105]。曾有过多种评估法[106],实践证明,RUCAM 仍是当前设计最合理、要素最全面、操作最方便、诊断准确率相对较高的 DILI 诊断工具[3,107]。其特点是:
(1)不受年龄、性别和种族影响,可重复性相对较好;(2)主次参数全面且相对合理客观;半定量诊断分析构架较为完整,也适合非肝病专业医生应用;(3)对不同类型 DILI 的评分标准进行了区分。其缺点是:有些评分标准的界定较含糊,需要改进参数和权重,填表指导应更清楚完整[105,108]。
有评估认为 Maria & Victorino 评估法[106,109]和 Naranjo 计分系统[110]均逊于 RUCAM。2004 年日本学者提出在改良 RUCAM 基础上增加药物淋巴细胞刺激试验(DLST)或称 LTT[111],但由于缺乏标准化和可重复性不够,其一直未获美国 FDA 批准。中华医学会消化病学分会肝胆疾病协作组于 2007 年推出一简要方案[112],其主要不足是将肝细胞损伤型和胆汁淤积型及混合型 DILI 混淆计分,并对 R 值作了不恰当的简化。最近美国提出的结构性专家观点程序(SEOP)[113],因程序繁琐而不适合临床广泛应用,但 可作为 DILI 临床研究及疑似病例进一步评估的工具。RUCAM 和 SEOP 之间的评估一致率存在差异[113]。
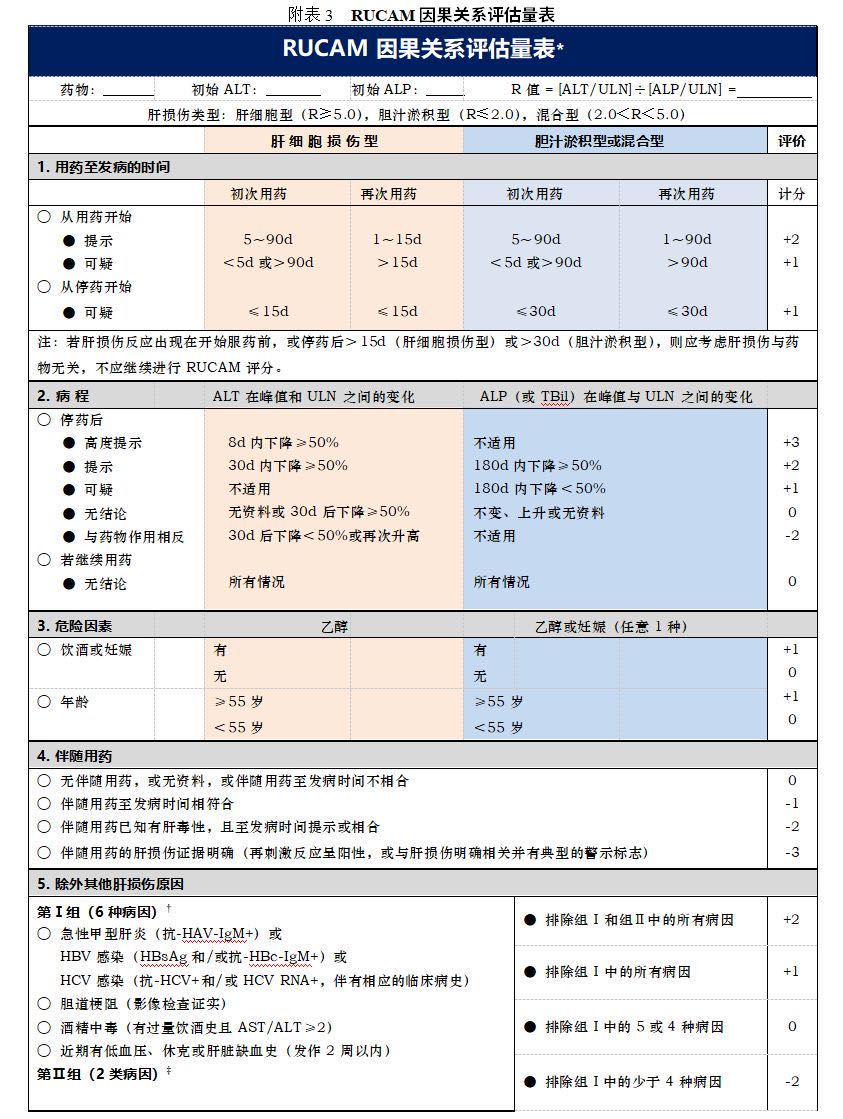
本指南推荐采用 RUCAM 量表(附表 3)对药物与肝损伤的因果关系进行综合评估:(1)用药史,特别是从用药或停药至起病的时间;(2)病程长短和生化异常的动态特点;(3)危险因素;(4)合并应用的其他药物;(5)肝损伤非药物性因素的排除或权重,以及血液生化异常非肝损伤相关因素的排除。对于需要排除的其他肝损伤病因,除了 RUCAM 量表已列出的 AIH、PBC、PSC、CHB 和 CHC 等疾病外,在我国还需排除急性戊型肝炎和发病率相对较低的 IgG4 胆管炎等疾病。(6)药物以往的肝毒性信息;(7)药物再激发反应。对难以确诊 DILI 的病例,必要时可行肝活检组织学检查。
RUCAM 量表根据评分结果将药物与肝损伤的因果相关性分为 5 级[105]。极可能(Highly probable):>8 分;很可能(Probable):6~8 分;可能(Possible):3~5 分;不太可能(Unlikely):1~2 分;可排除(Excluded):≤0 分。
SEOP 评估结果分为 6 级。明确 (Definite):量化可能性>95%,排除任何合理的怀疑;极可能 (Highly likely):量化可能性 75%~95%,证据清楚或令人信服,但并不确定;很可能 (Probable):量化可能性50%~74%,证据优势支持存在因果关系;可能 (Possible):量化可能性 25%~49%,证据优势不支持因果关系,但不能排除可能性;不太可能 (Unlikely):量化可能性<25%,根据现有证据高度提示不太可能;信息不足 (Insufficient information):因缺乏关键证据而无法进行有意义的评分。
(三)诊断流程
DILI 的诊断流程参见图 2。
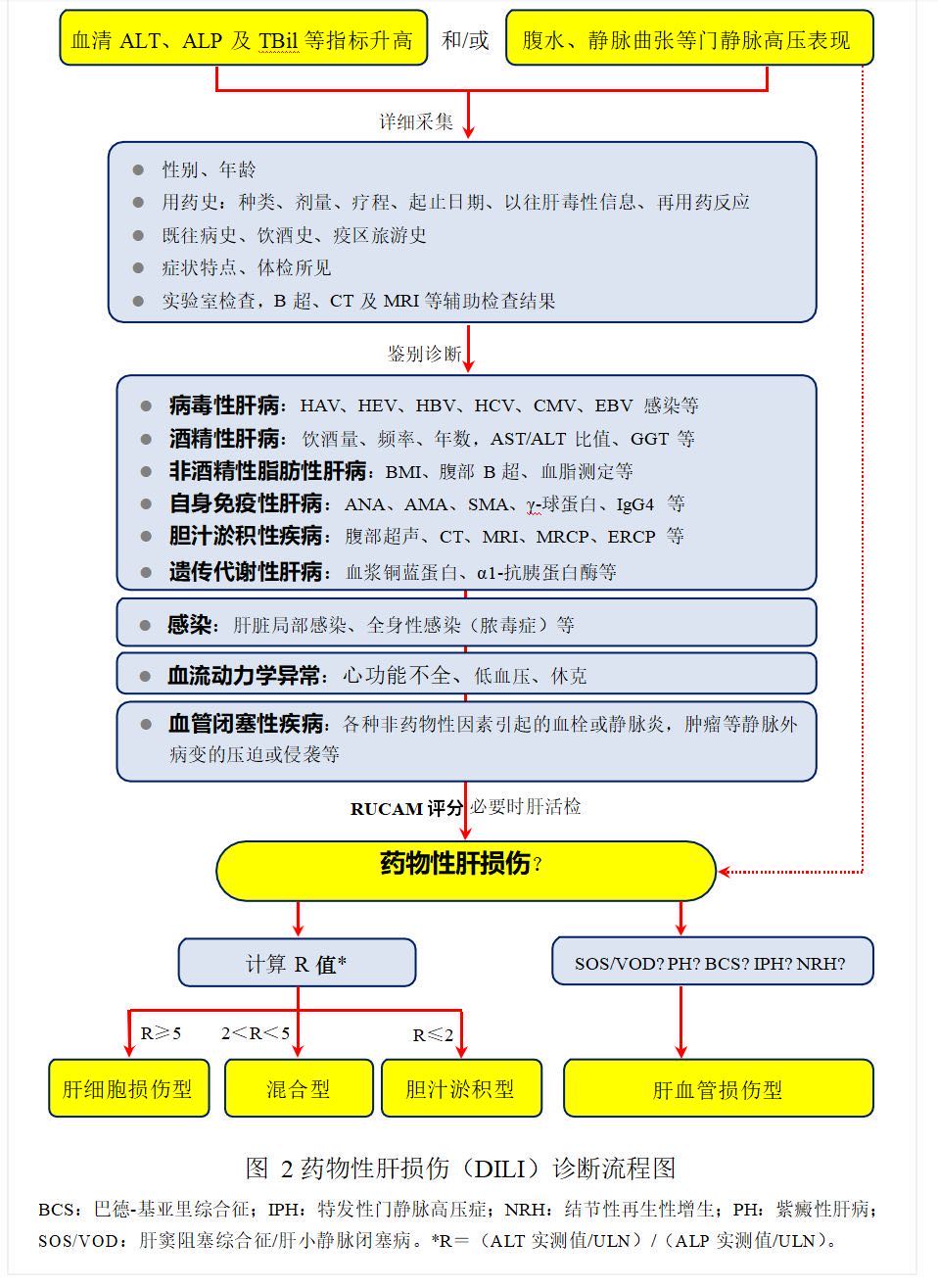
(四)DILI 严重程度分级
目前国际上通常将急性 DILI 的严重程度分为 1~5 级[92]。美国 DILIN 前瞻性研究[2,82]对其进一步数据化。结合我国肝衰竭指南,对分级略作修正:
l 0 级(无肝损伤):患者对暴露药物可耐受,无肝毒性反应。
l 1 级(轻度肝损伤):血清 ALT 和/或 ALP 呈可恢复性升高,TBil<2.5 ULN(2.5 mg/dL 或 42.75μmol/L),且 INR<1.5。多数患者可适应。可有或无乏力、虚弱、恶心、厌食、右上腹痛、黄疸、瘙痒、皮疹或体质量减轻等症状[3,114]。
l 2 级(中度肝损伤):血清 ALT 和/或 ALP 升高,TBil≥2.5 ULN,或虽无 TBil 升高但 INR≥1.5。上述症状可有加重。
l 3 级(重度肝损伤):血清 ALT 和/或ALP升高,TBil≥5 ULN(5 mg/dL 或 85.5 μmol/L),伴或不伴 INR≥1.5。患者症状进一步加重,需要住院治疗,或住院时间延长。
l 4 级(ALF):血清 ALT 和/或 ALP 水平升高,TBil≥10 ULN(10 mg/dL 或 171 μmol/L)或每日上升≥1.0 mg/dL(17.1 μmol/L)[115],INR≥2.0 或 PTA<40%,可同时出现(1)腹水或肝性脑病;或(2)与 DILI 相关的其他器官功能衰竭。
l 5 级(致命):因 DILI 死亡,或需接受肝移植才能存活。
(五)DILI 的规范诊断格式
完整的 DILI 诊断应包括诊断命名、临床类型、病程、RUCAM 评分结果、严重程度分级。诊断举例:
l 药物性肝损伤,肝细胞损伤型,急性,RUCAM 9 分(极可能),严重程度 3 级。
l 药物性肝损伤,胆汁淤积型,慢性,RUCAM 7 分(很可能),严重程度 2 级。
(六)鉴别诊断
1. 鉴别诊断要点 DILI 临床表型复杂,几乎涵盖目前已知的所有急性、亚急性、慢性肝损伤表型。排除其他肝病对建立 DILI 诊断有重要意义。为此,需通过细致的病史询问、症状、体征和病程特点、病原学检查、生化学异常模式、影像学乃至病理组织学检查等,与各型病毒性肝炎(特别是散发性戊型肝炎)、NAFLD、酒精性肝病、AIH、PBC、肝豆状核变性、α1 抗胰蛋白酶缺乏症、血色病等各类肝胆疾病相鉴别。
对于应用化疗药物或免疫抑制药物且合并 HBV 或 HCV 标志物阳性的患者,若出现肝功能异常或肝损伤加重,应注意鉴别是 HBV 或 HCV 再激活,还是化疗或免疫抑制药物所致的肝损伤,抑或两者兼而有之[116]。对正在接受 ART 的 AIDS 患者,若合并 HBV 或 HCV 标志物阳性且出现肝损伤,也应注意 ART 所致肝损伤与肝炎病毒复制再激活所致肝损伤之间的鉴别。
此外还应排除感染、中毒、心力衰竭、低血压或休克、血管闭塞以及肺功能不全等引起的全身组织器官缺氧性损伤。需注意 SOS/VOD 可以腹水为首发临床表现。
2. 与 AIH 等的鉴别 少数 DILI 患者因临床表现与经典 AIH 相似,可出现相关自身抗体阳性,临床较难与经典 AIH 鉴别。下列三种情况需特别注意:(1)在 AIH 基础上出现 DILI;(2)药物诱导的 AIH(DIAIH);(3)自身免疫性肝炎样的 DILI(AL-DILI)。AL-DILI 最多见,是指肝损伤同时伴有血清免疫球蛋白显著升高,抗核抗体(ANA)、抗平滑肌抗体(SMA)、抗肝肾微粒体抗体-1(LKM-1)阳性,偶见抗线粒体抗体(AMA)阳性;往往呈慢性病程,表现为 AIH 样症状,但急性发作也可致肝功能衰竭, 对糖皮质激素应答良好且停药后不易复发,支持 AL-DILI 的诊断。肝组织学同样也为鉴别 AL-DILI 和经典 AIH 的主要手段之一[117, 118],AIH 特征性组织学表现包括浆细胞浸润、肝细胞呈“玫瑰花环”样改变, 以及淋巴细胞穿入(emperipolesis) 现象;而汇管区中性粒细胞和嗜酸性粒细胞浸润及肝细胞胆汁淤积等更多见于 AL-DILI[117, 118]。
对初次发病、用药史明确、自身免疫特征明显而不能确诊者,在停用可疑药物后,可考虑糖皮质激素治疗,病情缓解后逐渐减量直至停药;随访过程中如无复发迹象则支持 DILI 诊断,若未再次用药而病情复发则多可诊断为 AIH[119]。
推荐意见:
1. DILI 临床诊断目前仍为排他性诊断,应结合用药史、临床特征和肝脏生化学指标动态改变的特点、药物再刺激反应、其他肝损伤病因的排除等进行综合分析。肝活检组织学检查有助于诊断和鉴别诊断。(1B)
2. 推荐 RUCAM 因果关系评分量表作为临床实践中 DILI 临床诊断的应用量表。>8 分为极可能(Highly probable),6~8 分为很可能(Probable),3~5 分为可能(Possible),1~2 分为不太可能(Unlikely),≤0 分为可排除(Excluded)。(1B)
3. 完整的 DILI 临床诊断应包括诊断命名、临床类型、病程、RUCAM 评分结果、严重程度分级。(1B)
4. 在自身免疫性肝炎(AIH)基础上发生的 DILI、药物诱导的 AIH 和伴有自身免疫特征的 AIH 样 DILI(AL-DILI)常难以鉴别。应详细采集用药史和分析自身免疫指标,动态观察临床治疗应答及免疫抑制剂停药后的反应,必要时行肝组织学检查加以鉴别。(2C)
5. 有基础肝病背景或存在多种肝损伤病因的患者,应用具有潜在肝毒性的药物时应注意更密切的监测。诊断 DILI 时应十分慎重,需排除原有肝病的发作和加重,仔细甄别肝损伤的最可能原因,以便正确治疗。(1B)
急性 DILI 患者大多预后良好。慢性 DILI 的预后总体上好于组织学类型相似的非药物性慢性肝损伤。胆汁淤积型 DILI 一般在停药 3 个月~3 年恢复[78];少数患者病情迁延,最终可出现严重的胆管消失及胆汁淤积性肝硬化,预后不良。韩国一项回顾性研究提示[144],213 例 DILI 患者其 30 d 短期预后不良的比例高达 13.1%,终末期肝病模型评分(MELD)和血红蛋白水平是患者短期预后的独立预测指标,而入院时肝损伤的临床类型(肝细胞损伤型、混合型或胆汁淤积型)与 30 d 短期预后的关系不大。
药物性 ALF/SALF 病死率高。美国 DILIN 多中心、前瞻性、大型队列研究初步结果显示[79],660 例药物相关性肝损伤成年患者,发病 6 个月内有 30 例患者接受了肝移植,32 例患者死亡,死亡病例中约53%与严重肝损伤直接相关。美国 ALF 研究小组收集的 133 例药物性 ALF 患者中,3 周内未行肝移植者生存率仅为 23%,接受肝移植者生存率为 42%[128]。
Hy’s 法则对判断 DILI 预后有重要参考价值。其核心内容是[3]:若一种药物在临床Ⅲ期试验中有患者出现血清 ALT 或 AST>3 ULN 和 TBil>2 ULN 的肝细胞性黄疸,则约 10%可发展为 ALF。在临床试验数据库中发现 1 例 Hy’s 法则案例是令人担心的,如出现 2 例就强烈提示该药在扩大人群的应用中可能引起严重的 DILI 问题[145]。地来洛尔临床试验中,1000 个受试者中出现了 2 例符合 Hy’s 法则的案例,因此未获美国 FDA 批准;后该药在葡萄牙上市,发现存在致命性肝损伤。他索沙坦临床试验中,因出现 1 例 Hy’s 案例而被要求上市前提供更多安全性数据,最终被放弃。新近欧美一项多中心、大样本研究显示[84],R 或 NR>5 对预测 DILI 的临床分型和重型 DILI 均有较大帮助。
推荐意见:
13. Hy’s 法则对判断 DILI 预后有重要参考价值。若在临床试验数据库中发现符合 Hy’s 法则的案例,应高度重视相关药物的肝毒性问题。(1B)
(一)预防和管理
我国人口众多,临床不规范用药较为普遍,医护人员和公众对 DILI 的认知和警惕性相当欠缺。另一方面,人群中普遍存在 TCM-NM-HP-DS 无害及自然植物无毒的观念。因此,DILI 防治形势较为严峻, 需要采用系统方法减少整体风险和增加获益。目前已有多种方法用于 DILI 的风险管理,主要包括:
(1)对药物肝毒性在说明书中给予黑框警示、警告和预防措施。
(2)上市后严密监测药物不良反应,在监测和评价过程中充分引入药物警戒理念[146]。我国现已建 成拥有 34 个省级药品不良反应监测中心、20 万基层用户和超过 660 万份个案报告的国家 ADR 监测系统,ADR 个案报告可通过基层单位自发上报,为其及时发现和快速应对提供了良好的技术和制度保障[147]。
(3)遵循临床指南合理用药[148-150]。控制药物处方量,避免滥用药物。
(4)用药期间定期进行肝脏生化学检测。
(5)加强用药知情同意管理,促使患者对 DILI 保持警觉。
(6)加强安全用药的公众健康教育,特别是要消除 TCM-NM-HP-DS 无肝毒性的错误认识。
如能开发出可靠的预测 DILI 的易感和损伤加重的新生物标志物并经验证和转化应用,将会对 DILI的风险管理有很大帮助。
(二)展望
LiverTox 和 HepaTox 等网络互动平台的建立和应用是近年来 DILI 研究领域的重大进展之一[7,8]。其提供的药物肝毒性信息、专业术语、诊断量表、最新资讯以及病例报告-管理-随访互动系统等,不仅大 大方便了医护人员和公众及时了解关于 DILI 的科学知识,充分警觉和规避 DILI 风险,同时也将对未来
DILI 的临床和基础研究产生重大影响和推动,重点包括:
(1)DILI 大数据库的构建、完善和合理应用。建立高灵敏的预测预警系统。
(2)开展更多术语定义明确、诊断标准统一、设计规范、具有良好可比性的大规模、多中心、前瞻 性、随机对照和合理干预的临床研究,推进对 DILI 病因、自然史、临床表型、治疗及预后的深入理解。
(3)应用基因组学、转录组学、蛋白组学及代谢组学等“组学(-omics)”技术评估 DILI 发病前后及个体之间相关遗传学、免疫学、分子生物学及生物化学事件的变化,对海量信息进行科学的统计处理, 探讨 DILI 信号转导及调控模式的特异性上游事件和非特异性下游事件的发生条件及其内在关联,推动对
DILI 发病机制的深入研究,并从中筛选具有良好敏感性和特异性的“DILI 易感性 BM”和“DILI 特异性 BM”,以便早期识别对特定药物的潜在易感者、适应者和耐受者,提高对 DILI 进行预测、预警、预防和诊断、评估及预后判断的准确性。
(4)不同病因所致肝损伤的共性和个性问题。
(5)基于新的诊断标志物研发新的 DILI 诊断量表或评估系统,突破目前方法的局限性。
(6)研发更适合中国人群的 DILI 生化学诊断标准,优化发生 DILI 后的停药标准。
(7)研发更为有效的 DILI 治疗药物和治疗模式。
推荐意见:
14. 据 DILI 风险管理的不同目标,采取不同的策略和方法,包括识别高风险患者、停药、减少剂量、监测基线和后续肝脏生化指标的改变,以及权衡整体获益和风险。(1B)
15. 临床医师应严格按照病情需要和药品说明书处方用药,充分注意药物配伍原则和配伍禁忌。加强针对公众的健康教育和风险管理,警惕 TCM-NM-HP-DS 的潜在不良反应,促使改变其安全无毒的错误观念,警惕民间偏方、验方及有毒植物等的肝毒性。(1B)
16. HepaTox 网站和 LiverTox 网站等网络互动平台的建立、发展、完善和应用有助于医药专业人员和公众对 DILI 的认知,在临床实践和科研中可充分加以运用。(1B)


转自微信公众号:药物性肝损伤
上一篇: 肝纤维化研究热点及进展—2019年视点
暂无数据